
2005.05.31
改正薬事法について
【改正の主な要点】
- 平成17年4月1日から法律的に「医療用具」から「医療機器」に名称を変更。
- 人体に対するリスクにより医療機器を分類(クラスⅠ~Ⅳ)。
- 販売業・賃貸業及び授与には取扱う機器によっては各営業所ごとに都道府県知事の許可が必要。これに伴い、販売業者・賃貸業者の安全対策がより厳しくなります。
【改正の要旨】
1.医療機器が不具合を起こした場合の人体へのリスクの大きさ別に下表の様に大別| 高度管理医療機器 クラスⅢ、Ⅳ |
管理医療機器 クラスⅡ |
管理医療機器 クラスⅠ |
| リスクが高い | リスクが比較的低い | リスクが比較的低い |
| 新たに許可が必要 | 届出が必要 | 届出不要 |
| ただし、「特定保守管理医療機器」についてはクラスに関係なく許可が必要 | ||
2.販売業・賃貸業に許可制を導入
※高度管理医療機器、特定保守管理医療機器、管理医療機器を取扱う場合、上図に示したとおり、「許可」若しくは「届出」が必要になります。 また、この時同時に特定の条件を満たした管理者を置く必要があります。
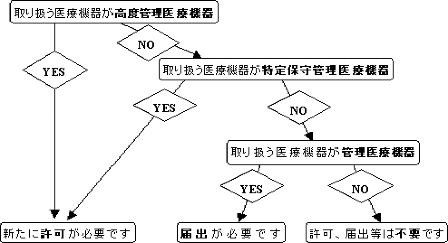
3.市販後安全対策の徹底
- 販売業者は品質に関して苦情や不具合が有った時、それが自らに起因しなければ、製造業者にその報告をしなければならない場合がある。
- 販売業者は品質などの理由で回収を行った場合、それが自らに起因する場合 適切な処置を行わなければならない。
- 販売業者等はその医療機器の有効性・安全性・適正使用に関する情報を収集提供に努めなければなりません。








